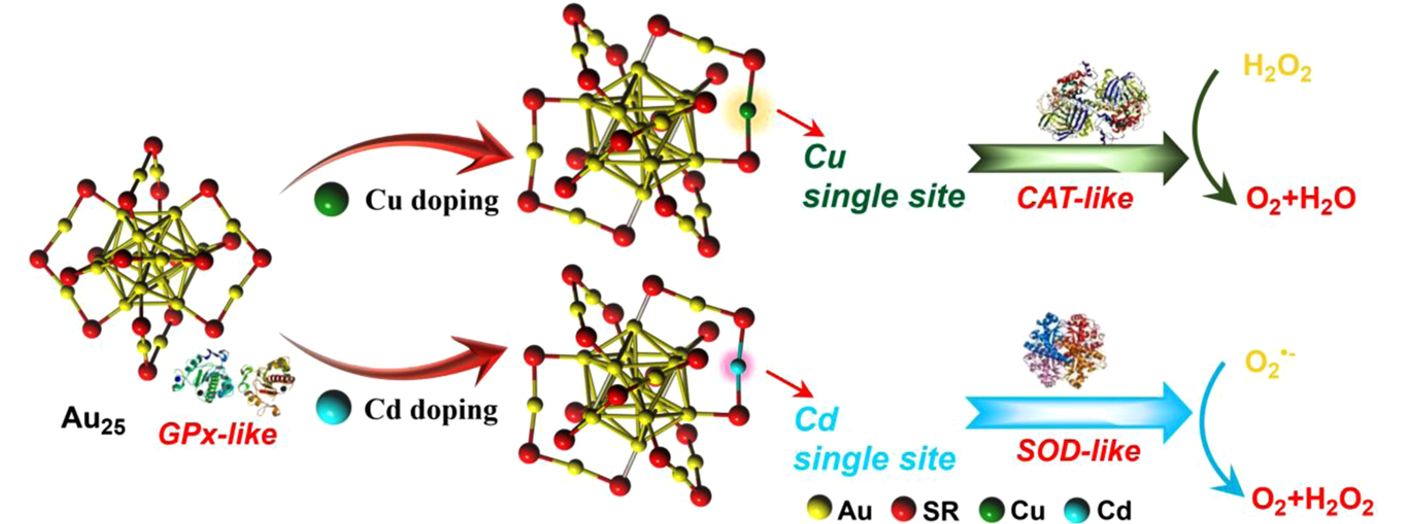
人工酶
与天然酶相比,人工酶表现出更优异的催化活性和更高的稳定性,通过表面修饰、原子掺杂等更容易提高催化特性。我们得到了一系列具有多酶活性的纳米材料(包括但不限于具有原子精度的团簇材料),如金纳米簇、单原子纳米酶等 (Nat. Comm., 12, 2021; Sci Adv, 7, 2021), 我们研究其催化特性及在重大疾病中的应用(Nano Lett, 21, 2021)。
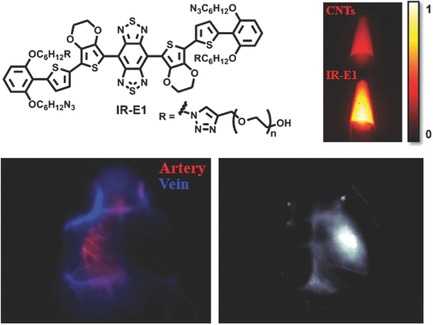
生物成像
由于较长波长的生物组织的光子散射减少,与近红外一区 成像 (750-900 nm) 相比,近红外二区窗口 (1,000-1,700 nm) 可用于深层组织荧光成像可用于亚厘米组织深度的无创体内成像,空间分辨率低于 10 微米 。 我们使用大型共轭系统作为电子供体以增强荧光并在近红外二区窗口(1100-1700 nm)设计了明亮的荧光分子,实现了高分辨率肿瘤成像(Adv. Mater. 28, 2016)和创伤性脑损伤成像(Adv. Mater. 31, 2019)。
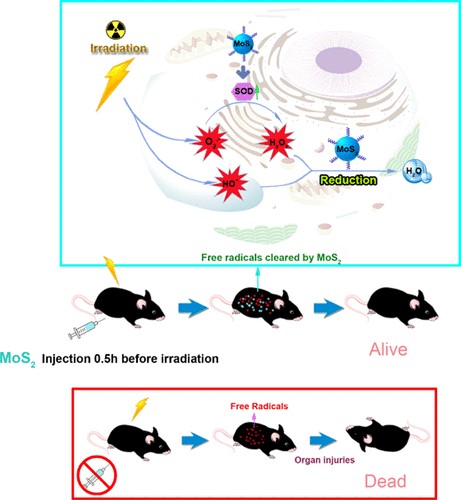
纳米药物
放疗被认为是肿瘤手术切除后治疗方案的一部分。 我们设计了一系列Au簇CT造影剂,如Au10、Au25、Au33,可以实现超高的肿瘤特异性(Adv. Mater., 26 ,2014; Adv. Healthcare Mater., 3 ,2014),高效的癌症辐射(Sci. Rep., 5 ,2015; Biomaterials, 33 ,2012)和肾脏清除率以及低毒性(Biomaterials, 33 ,2012; Small, 11, 2015)。我们建议放射物理学与分子工程相结合可以作为放射治疗期间筛选高性能放射防护生物材料的设计策略(ACS Nano, 10, 2016; ACS Biomat. Sci. Eng., 3, 2017)。
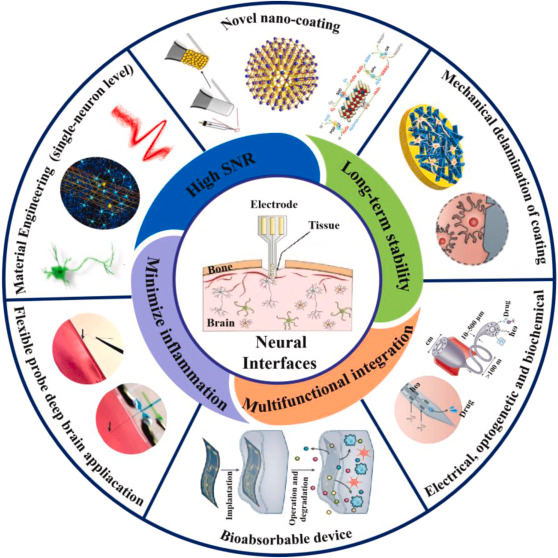
神经电极
我们设计与构建了高效催化的人工酶电极,研究电极材料与生物组织界面的电子界面传输过程以及组织界面的炎症调控过程。 我们致力于解决神经植入电极的生物相容性差、灵敏度低、难以长期采集等难题。我们倾向于建立人工酶电极设计与应用的新技术体系,推动植入电极临床转化,并且为其它生物植入材料提供理论和技术支撑 (Biosens. Bioelectron. 170, 2020)。
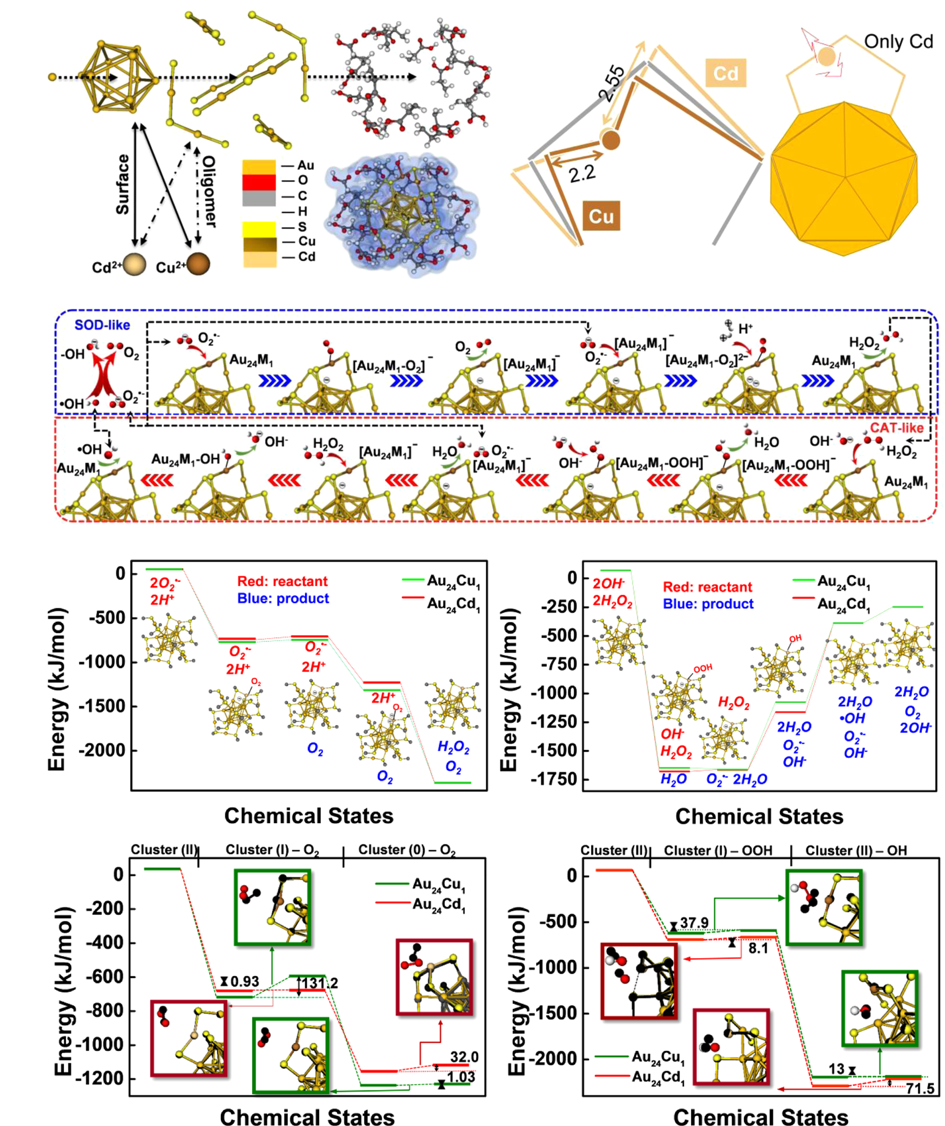
计算
基于第一性原理计算,具体包括以下几个方向:
1. 基于密度泛函(DFT)和含时密度泛函理论(TDDFT)的金属-有机纳米团簇的结构及其光学性质的模拟。金属和金属化合物团簇的红外光谱模拟。
2. 纳米酶的催化反应机理的探究。
3. 机器学习算法和第一性原理相结合下的新材料开发模拟。特别是强化学习和量子理论相结合的探索。